



近年来,光动力治疗(PDT)作为一种非介入性治疗手段因其选择性高,负作用小而被广泛用于临床抗肿瘤治疗。
在中科院、国家自然科学基金委和科技部的资助下,国家纳米科学中心纳米生物效应与安全性院重点实验室的李峻柏、杨洋课题组长期致力于纳米生物材料的组装与抗肿瘤的光动治疗临床应用研究,并取得了系列研究进展。在提高光动治疗效率方面,该课题组通过将具有携氧功能的血红蛋白或可催化产氧的过氧化氢酶组装到纳米生物材料中,并同时负载光敏剂为PDT提供额外的氧气以提高治疗效率(Adv. Funct. Mater. 2012, 22, 1446-1453; Adv. Healthcare Mater. 2018, 1701357;ACS Nano 2018, 12, 1455-1461)。在提高光动治疗深度方面,课题组通过双光子激光成像,将双光子染料与光敏剂同时组装成纳米生物材料,在双光子激发下在纳米材料内部发生intraparticle FRET效应,提高了传统光敏剂的双光子吸收而提升治疗深度(Angew. Chem. Int. Ed. 2016, 55, 13538-13543, back cover highlight;Adv. Funct. Mater. 2016, 26, 2561-2570;Chem. Commun. 2018, 54, 715-718, front cover highlight)。
基于上述工作基础,他们优化材料设计方案,通过分子组装技术,将血红蛋白、双光子染料与光敏剂共组装成单分散的纳米颗粒,进一步在其粒子表面包覆含有高选择性探针分子的磷脂膜,经过活体抗肿瘤实验,在双光子作用下,显著提升了PDT治疗效率与治疗深度,为解决传统PDT抗肿瘤应用中面临的难题提供了新途径,相关工作发表在Angew. Chem. Int. Ed. 2018,DOI:10.1002/anie.201802497。
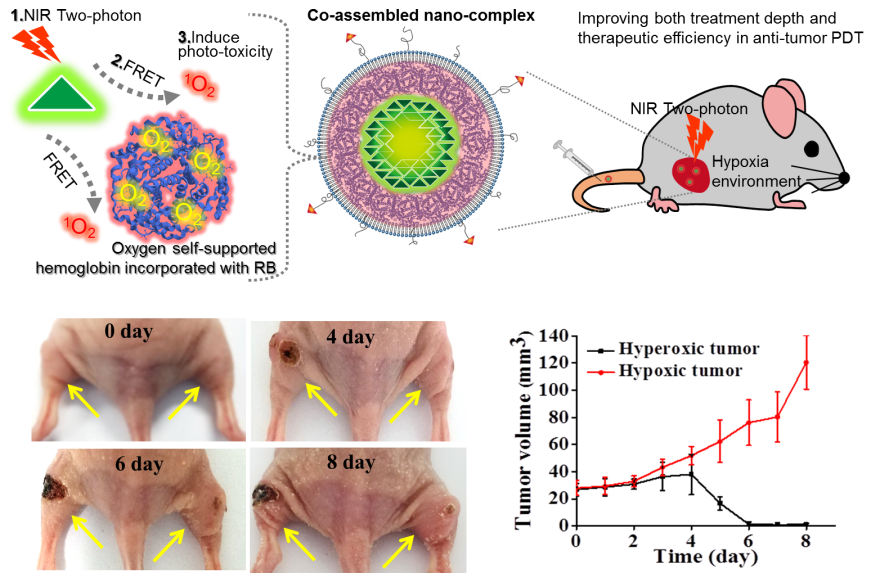
图 组装的纳米生物材料可高校提升光动治疗深度和治疗效率