近日,国家纳米科学中心李乐乐课题组在基因/药物共递送研究中取得重要进展,相关研究成果“A Biomimetic Coordination Nanoplatform for Controlled Encapsulation and Delivery of Drug-Gene Combinations”发表在《德国应用化学》杂志上 (Angew. Chem., Int. Ed. 2019, DOI: 10.1002/anie.201903417)。该研究成果还被《德国应用化学》的高级副主编推荐到国际学术网站平台ChemistryViews.org上作为研究亮点(Research Highlight)报道。
基因和小分子药物的共递送策略是当前肿瘤治疗的新方向,在临床中广泛使用。近年来,研究人员开发出了多种基因与小分子药物共载纳米载体以提高其递送效率,如阳离子脂质体、聚合物胶束、无机纳米粒等。然而,受限于核酸药物和小分子药物迥异的理化性质,现有的纳米共载载体存在以下问题:(1)合成过程复杂,往往需要多个繁琐的步骤来实现纳米载体的制备以及两种药物的装载;(2)药物共载效率低,导致了药物在装载过程中的浪费;(3)药物装载含量低,给药时外源材料在体内的大量引入带来安全性问题。因此,发展一种简单高效的共载策略,实现基因和小分子药物在单个纳米颗粒中的可控装载以及高效递送,仍然是药物协同治疗领域一个难题。
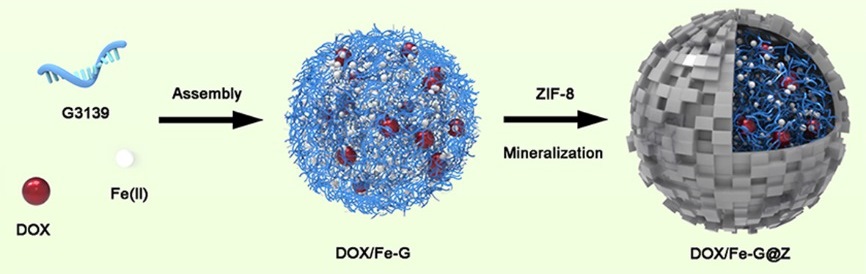
最近,受自然界生物矿化的启发,国家纳米科学中心李乐乐课题组开发出一种简单、普适的仿生方法,实现了基因和小分子化疗药物的高效共载和磁共振成像介导的肿瘤协同治疗。该纳米共载体系制备方法非常简便和快捷,两种药物分子与铁离子通过配位驱动的一步自组装,即可形成形貌规则的纳米结构;随后的的表面矿化可有效提高其生物稳定性。重要的是,该共载体系不仅具有高的药物共载效率和含量,而且两种药物分子的担载比例精确可调。同时,铁离子的引入使得该体系可用于磁共振成像介导的活体示踪。研究表明,作为一种新颖的、无载体的共递送体策略,该共载体系可将核酸药物和小分子药物有效的递送到肿瘤中,实现磁共振成像介导的肿瘤协同治疗。该工作为基因/药物共递送以及诊疗一体化开辟了一种新的方法学。
论文链接:https://onlinelibrary.wiley.com/doi/pdf/10.1002/anie.201903417