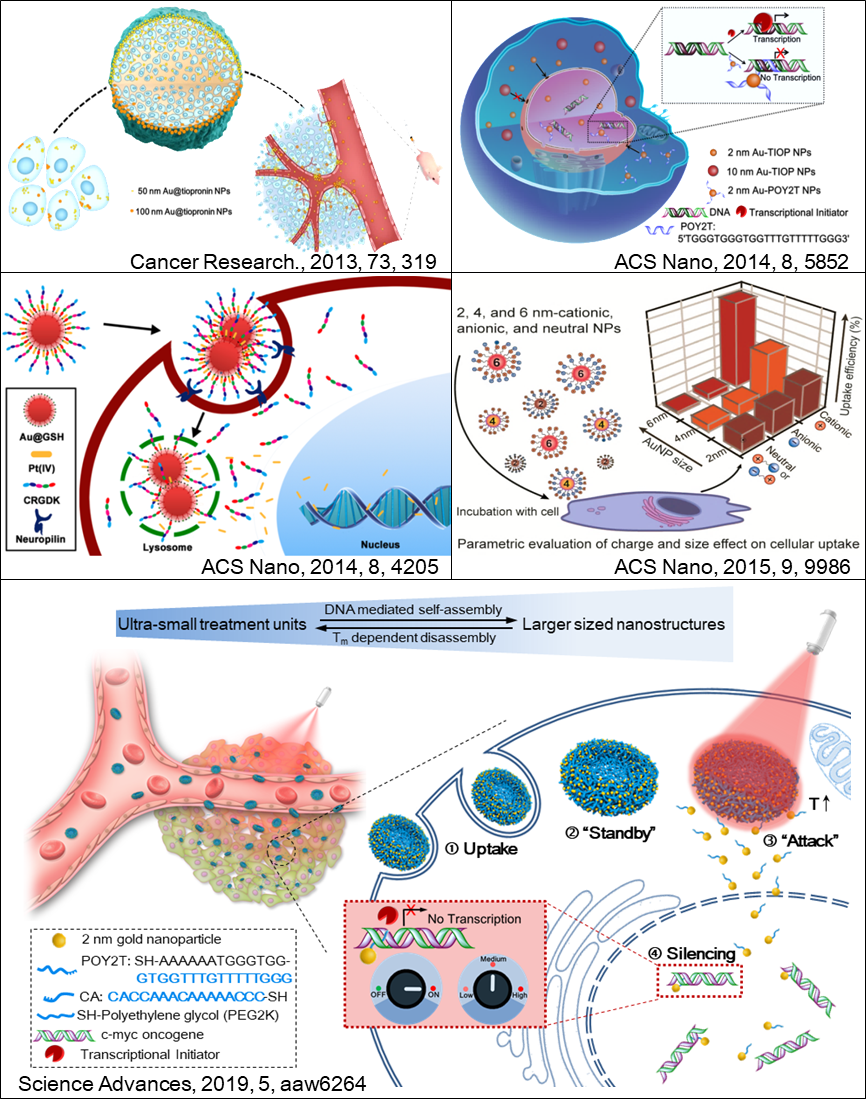
2019年10月2日上线的最新一期Science Advances(《科学-进展》)杂志在线发表了国家纳米科学中心梁兴杰课题组在可控基因治疗纳米药物领域的研究进展“Gold-DNA nanosunflowers for efficient gene silencing with controllable transformation”。该工作不仅为构建可变形纳米载体用于调控基因表达提供了新策略,而且为Au纳米药物的成药性研究提供了新的佐证。
近年来,梁兴杰课题组一直围绕纳米药物在生物体系中的构效机制开展相关研究,旨在优化纳米药物的成药性并且用于临床研究。前期的一系列研究表明:尺寸较小的纳米药物颗粒在肿瘤组织的渗透和摄取方面显示出更多优势,同时具有更长的体内循环时间;而尺寸较大的纳米药物颗粒具有更优的被动靶向效果,其中50 nm左右的药物颗粒在实现肿瘤被动靶向的同时,也具备良好的肿瘤穿透效果。相关研究成果进一步明确了该领域多年来关于纳米药物在实体肿瘤部位是否存在尺度效应的争论,为纳米药物及载体的设计提供了重要依据和指导性参考(ACS Nano, 2012, 6, 4483; Cancer Research, 2013,73, 319)。
此外,梁兴杰课题组着重研究了小尺寸纳米药物颗粒在生物体系中的作用规律和生物学机制,填补了该领域对小尺寸纳米药物的内吞机制、细胞核靶向、体内分布代谢等纳米生物学规律的系统研究空白,为选择性调控肿瘤细胞与纳米药物的相互作用研究奠定了重要基础(ACS Nano, 2014, 8, 5852; ACS Nano, 2015, 9, 9986; Bioconjugate Chemistry, 2017, 28, 1, 239)。与此同时,该课题组还开发了一系列用于癌症治疗的新型Au纳米药物及载药系统,实现了:将铂类药物靶向输送到前列腺癌细胞(ACS Nano, 2014, 8, 4205)、高效的细胞核靶向(ACS Nano, 2014, 8, 5852)、线粒体靶向(Nature Nanotechnology, 2019, 14, 379)等重要研究成果。
基于前期的一系列研究,该课题组的研究人员综合考虑了纳米药物颗粒在体内的多种生物学行为特性,打破常规,设计构建了可变形的多级次纳米药物递送系统(NanoSunflowers),结合体外近红外光的调控响应,同时实现了:大尺寸颗粒(~200 nm)被动靶向到肿瘤部位,中等尺寸颗粒(~50 nm)渗透进肿瘤内部,小尺寸颗粒(<10 nm)被肿瘤细胞高效摄取,最终实现了良好的基因调控效果。该研究成果受到了期刊编辑和审稿人的一致好评(Science Advances, 2019, 5, aaw6264)。
国家纳米科学中心已毕业学生霍帅东博士和宫宁强博士为该研究论文的共同第一作者,霍帅东博士和梁兴杰研究员为共同通讯作者。该研究得到了国家重点研发计划,国家自然科学基金委和中科院国际合作等项目的支持。
原文链接:https://advances.sciencemag.org/content/5/10/eaaw6264