近日,国家纳米科学中心李乐乐、赵宇亮课题组在上转换介导的光动力治疗方面取得重要进展。相关研究成果“Nd3+-Sensitized Upconversion Metal-Organic Frameworks for Mitochondria-Targeted Amplified Photodynamic Therapy”发表在《德国应用化学》上 (Angewandte Chemie International Edition, 2019, DOI: 10.1002/anie.201911508)。
光动力疗法(PDT)是一种基于光化学反应的治疗技术,具有高的可控性和低的毒副作用,已被应用于肿瘤等相关疾病的临床治疗。然而,临床批准的光敏剂需要可见光来激发,其有限的组织穿透能力制约了光动力疗法在深层肿瘤治疗上的应用;此外,复杂的生理和病理屏障制约了光敏剂在亚细胞水平的空间特异性分布,无法有效地发挥ROS的毒性。团队前期一直致力于发展上转换发光介导的“时-空”可控的纳米生物技术,并探索其在精准生物检测和疾病诊疗方面的应用(Nat. Commun. 2019, 10, 2839;J. Am. Chem. Soc. 2019, 141, 7056;Angew. Chem. Int. Ed. 2019, 58, 14877;J. Am. Chem. Soc. 2018. 140, 578;J. Am. Chem. Soc. 2017, 139, 13804)。最近,团队通过引入光开光分子,开发了一种光致变色上转换纳米光敏系统,实现了双波长近红外光编程的精准光动力治疗,相关成果以封面文章发表在Chemical Science (2019, 10, 10231-10239)。
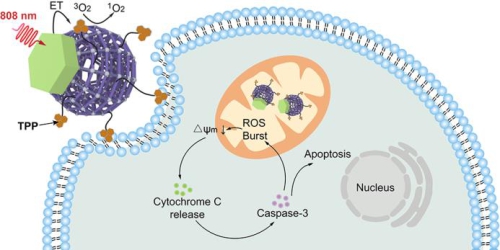
在前期工作的基础上,我们设计构建了Nd3+离子敏化的上转换金属有机框架Janus纳米结构,实现了近红外光触发的、精准靶向线粒体的放大型光动力治疗。该团队利用外延生长法合成了Nd3+离子掺杂的、具有核壳结构的上转换纳米粒子(UCNPs)作为晶种,然后通过界面诱导的自组装策略控制卟啉类金属有机框架材料(MOFs)在其表面各向异性生长,制备了具有Janus(古罗马神话中的两面神的名字)结构的纳米光敏剂;进一步利用结构不对称的特性对其进行表面功能化,赋予其对线粒体的靶向特异性。在808 nm近红外光激发下,Janus纳米光敏剂中UCNP捕获低能量光子后,通过共振能量转移将能量传递给临近的MOF纳米粒子,从而特异性的在线粒体内产生单线态氧,实现光动力治疗。重要的是,通过亚细胞水平调控线粒体(细胞的动力源和自杀武器储藏库)中ROS动态平衡,可激活细胞死亡机制来放大光动力治疗效果。此外,808 nm激发光的使用可有效避免传统980 nm激发上转换发光所产生的热效应和损伤正常组织的问题,提高了激光应用的安全性。该工作为肿瘤的高效光动力治疗提供了一种新思路,将近红外光激活技术与精确的空间控制技术相结合,是下一代PDT系统的发展新方向。
国家纳米科学中心联合培养硕士研究生刘畅、刘蓓博士和赵健副研究员为该论文的共同第一作者,李乐乐研究员和赵宇亮院士为共同通讯作者。该研究得到了国家人才计划和国家自然科学基金等项目的支持。
论文链接:https://www.onlinelibrary.wiley.com/doi/pdf/10.1002/anie.201911508。