



近日,国家纳米科学中心陈春英课题组在利用乏氧组装的超小氧化铁纳米颗粒放大肿瘤的荧光和磁共振成像信号方面取得重要进展。相关研究成果“Hypoxia-Triggered Self-Assembly of Ultrasmall Iron Oxide Nanoparticles to Amplify the Imaging Signal of a Tumor”以Supplementary Cover文章发表于《美国化学会志》(J. Am. Chem. Soc. 2021, DOI: 10.1021/jacs.0c10245)。
乏氧在实体瘤中非常普遍,对肿瘤的发生、发展、转移和治疗耐受有重要影响,其可以作为治疗预后的一个单独指标。因此,对肿瘤病人的乏氧程度进行预测和评估对于治疗效果的评价和治疗方式的选择具有不可忽视的作用。然而,乏氧区位于肿瘤中远离血管的部位,传统的造影剂很难在此区域进行富集和长效滞留,对于该区域的成像造成了极大的障碍。这一现象对纳米造影材料的渗透性提出更高的设计要求。
陈春英课题组及其合作团队长期致力于肿瘤乏氧的基础与转化研究,在增强纳米颗粒的肿瘤渗透性、改善肿瘤诊疗效果等方面取得系列进展 (Nano Today 2020, 34, 100907; Science Advance 2019, 5, eaax0937; Advanced Materials, 2020, 2006189; Angew Chem, 2020, 59: 14014-14018; Advanced Materials, 2016, 28, 8950)。课题组近期研究获得的乏氧组装氧化铁纳米颗粒,展现了良好的肿瘤渗透性,以及靶向肿瘤乏氧区域的能力,继而有效地放大肿瘤的荧光与磁共振成像信号,为乏氧肿瘤的评估提供新方法。
超小氧化铁纳米颗粒 (UIO) 具有尺寸均一、形貌规整、安全性高和制备方法成熟等优点,是核磁共振T2加权成像造影剂的首选。本研究将硝基咪唑衍生物(Pimo) 作为乏氧触发器修饰在UIO纳米颗粒表面,构建乏氧探针UIO-Pimo。超小尺寸能帮助UIO-Pimo渗透至肿瘤乏氧区;同时,Pimo在乏氧环境、电子供体和硝基还原酶的共同作用下进行生物还原反应,触发大尺寸组装体的形成,提升T2成像信号,增强其所在肿瘤乏氧区磁共振造影的检测灵敏度。据此,本工作还建立了MRI差值法,获得乏氧肿瘤在活体中的三维分布,为该方法的临床应用奠定基础。UIO-Pimo探针同时载带了疏水环境诱导荧光信号增强的NBD分子,该组装体进而实现了增强的荧光信号探测。本研究的乏氧组装策略,能够大大提高纳米颗粒在肿瘤部位的浓度和滞留时间,为克服纳米材料渗透能力有限所带来的治疗局限性提供新的解决方法。
国家纳米科学中心助理研究员周会鸽、博士研究生郭梦雨和特聘研究员李佳阳为该文章的共同第一作者,陈春英研究员为通讯作者。上述研究工作得到了科技部、国家自然科学基金委员会、中科院战略性先导科技专项 (B类)等项目的支持。
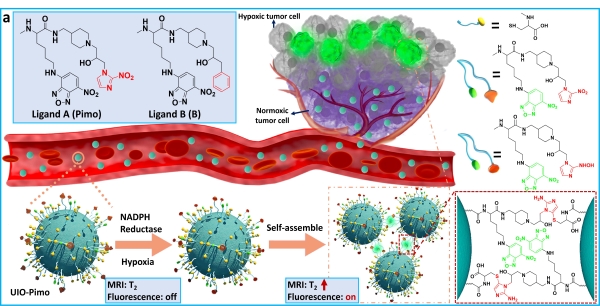
图:乏氧触发超小氧化铁纳米颗粒组装并放大荧光与核磁成像信号