



近日,国家纳米科学中心高兴发团队在医用纳米材料理论研究方向取得系列进展。相关成果以Computer-aided nanodrug discovery: recent progress and future prospects和Optimizing the standardized assays for determining the catalytic activity and kinetics of peroxidase-like nanozymes为题,分别发表于Chemical Society Reviews(10.1039/D3CS00575E)和Nature Protocols (10.1038/s41596-024-01034-7)。团队综述了医用纳米材料设计的最新研究动态,并展望了未来发展方向,强调了计算辅助设计和标准化实验方法在推动该领域发展中的关键作用。
纳米材料因其独特的物理化学特性,在疾病预防和治疗方面展现出了重大潜力。然而,面对众多的纳米材料种类和复杂的纳米-生物界面相互作用,实现具有特定生物医学功能的纳米材料的精准设计和筛选仍然面临挑战。计算机集群和算法的快速发展为实现这一目标提供了契机。研究团队深入探讨了计算机辅助医用纳米材料发现的潜力,特别强调了计算方法在揭示纳米材料与生物分子间关键界面相互作用——包括表面吸附、超分子识别、表面催化和化学转化——的核心作用。这些相互作用是决定纳米材料医学功能的关键因素(图1)。此外,团队还探讨了机器学习技术如何通过分析大量实验和计算数据,预测纳米材料的医学功能,为个性化精准医疗提供了新途径。这种跨学科的创新整合不仅极大加速了医用纳米材料的研发进程,更为未来精准纳米药物的设计和筛选提供了强有力的技术支持,有望实现更高效、更安全的治疗方式,满足临床治疗的个性化需求。
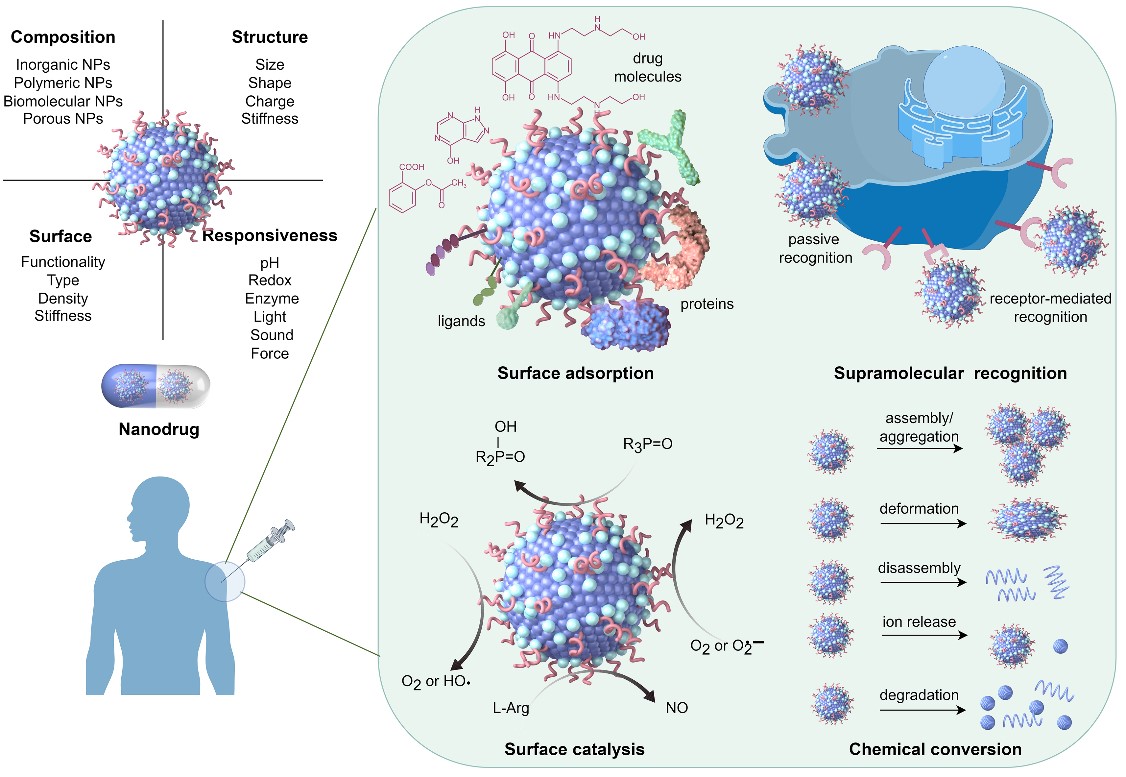
图1. 医用纳米材料理化性质及影响其医学功能的纳米-生物界面相互作用(由Figdraw绘制)。
纳米材料的类酶催化活性是其生物医学应用的一个关键特征。为了促进具有类酶催化活性的医用纳米材料的发展,需要精确调控其活性位点的几何和电子结构,以优化催化活性和底物选择性。因此,对这类纳米材料的催化活性和动力学特性的准确表征变得至关重要。为此,高兴发团队与北京理工大学梁敏敏教授团队合作,提出了一种改进的标准化方法。该方法结合了传统酶的米氏动力学和纳米材料的理化性质,能够更准确地描述不同形状、尺寸和组分的类过氧化物酶纳米材料的动力学活性(图2)。这一方法不仅有助于全面评估不同类酶催化纳米材料的酶学特性,还对于推动这些医用纳米材料在实际应用中的发展具有重要意义。考虑到现有的催化活性测定技术和活性位点数量及表面积的测量技术已相对成熟,这种优化的表征方法有望在纳米医学领域得到更广泛的应用,为设计和筛选具有特定生物医学功能的纳米材料提供强有力的实验支持。
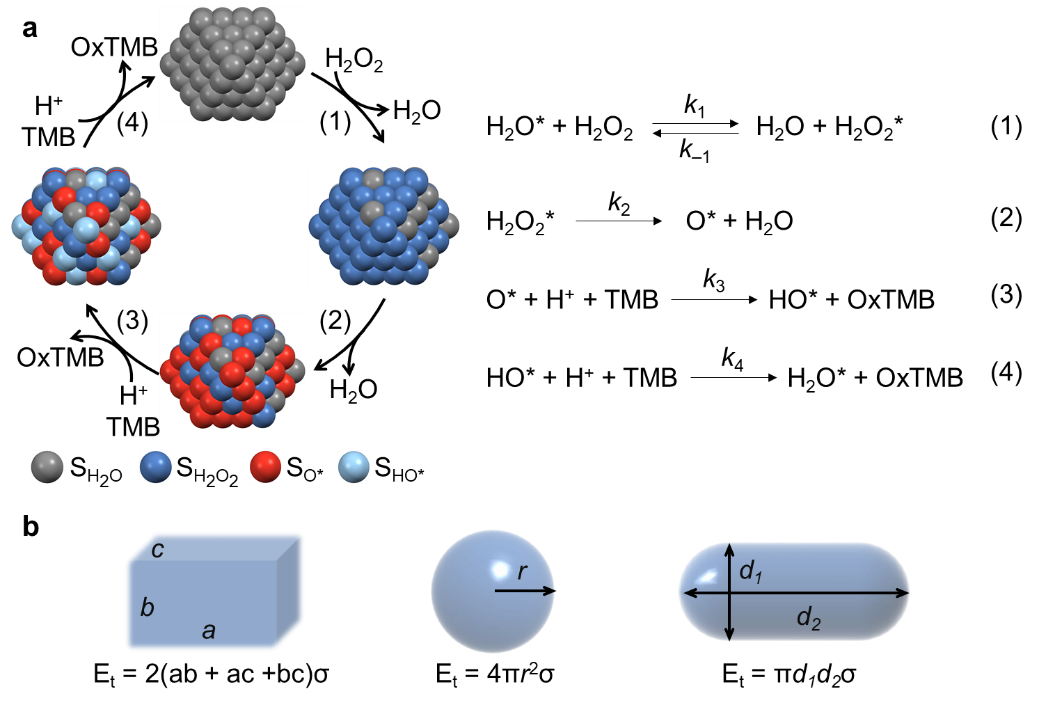
图2. 不同理化性质的类过氧化物酶纳米材料催化反应路径。
国家纳米科学中心征甲甲副研究员为论文Chemical Society Reviews的第一作者,高兴发研究员为通讯作者;国家纳米科学中心征甲甲副研究员、北京理工大学Feiyan Zhu为论文Nature Protocols的共同第一作者,北京理工大学梁敏敏教授、国家纳米科学中心高兴发研究员及北京理工大学贺久洋博士为共同通讯作者。该系列工作得到了基础科学中心、重点研发计划及国家自然科学基金等项目的资助。
论文链接:
https://pubs.rsc.org/en/content/articlelanding/2024/cs/d3cs00575e
https://www.nature.com/articles/s41596-024-01034-7