



近日,国家纳米科学中心朱墨桃研究团队联合北京大学第一医院杨尹默教授团队,在胰腺癌肿瘤新抗原疫苗研究中取得进展。该研究巧妙利用药物诱导的“异源自噬”机制,将肿瘤内天然定植的益生菌转化为新抗原来源,开发出一种全新的“菌源”疫苗策略,为胰腺癌等免疫治疗耐药肿瘤提供了新的治疗思路。相关研究成果以“Leveraging intratumoral probiotics for pancreatic cancer immunotherapy via xenophagy”为题,发表于Cell Host & Microbe。
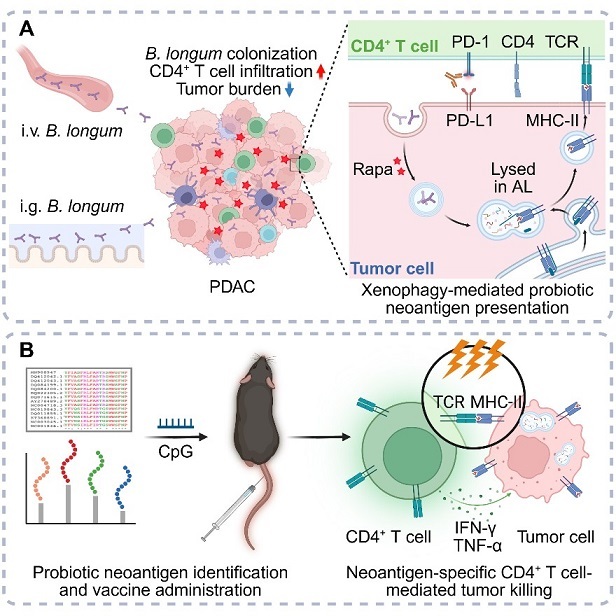
胰腺导管腺癌(PDAC)素有“癌症之王”之称,其肿瘤“免疫荒漠”状态导致免疫治疗屡屡受挫。如何将“冷”肿瘤转化为“热”肿瘤,激活免疫系统识别并攻击癌细胞,是胰腺癌免疫治疗的核心难题。本研究从临床问题出发,首先对40例PDAC患者肿瘤组织进行16S rDNA测序,发现双歧杆菌属是瘤内丰度较高且具有抗肿瘤潜力的优势菌群。进一步筛选证实,长双歧杆菌(B. longum)具备最优的肿瘤细胞侵入效率,能特异性靶向并定植于胰腺肿瘤内部。团队利用低剂量雷帕霉素诱导肿瘤细胞启动“异源自噬”——一种选择性清除胞内病原体的自噬机制。这一过程促使肿瘤细胞“消化”入侵的长双歧杆菌,将其蛋白片段递呈到细胞表面的MHC II类分子上,形成全新的“细菌来源新抗原”,从而将原本“隐身”的瘤内菌变为免疫系统可识别的“显形”目标,团队将这一策略命名为XenoPro。
在小鼠胰腺癌原位模型中,XenoPro策略显著抑制肿瘤生长。机制研究表明,异源自噬促进了胞内菌降解,上调了肿瘤细胞MHC-II分子表达,并诱导以CD4⁺ T细胞为主导的免疫识别。基于前期在抗原筛选与佐剂设计方面的积累,团队进一步从长双歧杆菌蛋白中筛选鉴定出12条高免疫原性MHC-II限制性新抗原,构建了治疗性多肽疫苗(Vax)。XenoPro与Vax联合应用在胰腺癌原位及肝转移模型中产生显著协同效应,显著延长小鼠生存期。这一联合策略在MC38结肠癌和B16-F10黑色素瘤模型中同样有效,展现了广谱抗肿瘤潜力。
为提升临床转化潜力,团队证实口服给予长双歧杆菌可达到与静脉注射相当的抗肿瘤效果,且安全性更优。XenoPro与抗PD-1抗体联合使用可进一步增强抗肿瘤疗效,并优化肠道菌群微环境,富集与免疫治疗正相关的有益菌属。本研究首次系统揭示了基于异源自噬的瘤内益生菌降解及“菌源疫苗”策略在胰腺癌免疫治疗中的应用价值。这一策略不依赖昂贵的患者特异性新抗原测序,而是利用可标准化生产的益生菌作为通用型新抗原库,为破解免疫治疗耐药肿瘤的临床困境提供了全新思路。
朱墨桃课题组长期致力于纳米疫苗技术研究。前期工作中,开发了共递送肿瘤抗原与TLR激动剂的硅微粒疫苗平台(J. Control. Release 2018);发现超小纳米颗粒可通过激活炎症小体,产生佐剂效应抗体产生(ACS Nano 2020);在益生菌介导的肿瘤治疗方面,团队近期开发了嗜黏蛋白阿克曼菌来源的工程化外膜囊泡用于癌症免疫治疗(Acta Pharm. Sin. B 2025,Adv. Sci. 2025, Nano Today 2023)。这些研究为本次“菌源疫苗”策略的提出奠定了坚实的理论与技术基础。
国家纳米科学中心朱墨桃研究员、北京大学第一医院院长杨尹默教授为论文共同通讯作者;北京大学第一医院李宝毅博士研究生、刘光年博士、朱昱博士研究生为论文共同第一作者。该研究工作得到了国家重点研发计划、国家自然科学基金等项目支持。
全文链接:https://www.cell.com/cell-host-microbe/abstract/S1931-3128(26)00078-8