



近日,国家纳米科学中心、中国科学院高能物理研究所、华南理工大学与北京大学联合团队,在纳米材料蛋白冠原位分析及受体发现方法学方面取得重要进展。相关研究成果以“Receptor discovery for nanomaterial soft and hard coronas via a biosensor-based Fishing strategy”为题,发表于方法学期刊Nature Protocols。该项研究构建了一套普适性强的实验体系,为解开纳米材料在活体内的生物识别密码提供了系统性的解决方案。
现代纳米医学正面临着一道核心的转化鸿沟:大量精心设计的靶向纳米药物,一旦进入血液或间质液,便会被迅速披上一层由蛋白质等生物分子组成的“蛋白冠”。这层内源性外衣赋予了纳米材料全新的生物学特征,直接主导其在体内的分布、清除、细胞摄取及免疫应答。这导致许多纳米药物在体内陷入“预期设计与实际表现不一致”的窘境,例如,聚乙二醇(PEG)化虽旨在延长纳米药物循环时间,但反复注射可能诱导产生抗PEG抗体,导致加速血液清除(ABC)效应;主动靶向配体(如抗体、多肽)也常因蛋白冠的遮蔽而丧失其识别能力。因此,破译蛋白冠调控受体识别的底层逻辑,已成为纳米医学临床转化的关键科学支点。
破解此谜题的最大障碍在于蛋白冠具有动态的分层结构,由结合紧密、相对稳定的“硬冠”与结合松散、高度动态交换的“软冠”构成。而传统研究方法(如超速离心、尺寸排阻色谱等)产生的强剪切力、机械挤压或缓冲液变化中极易导致软冠崩解和关键组分信息丢失。针对上述挑战,团队创新性地发展出基于生物膜层干涉技术的“垂钓(Fishing)”策略。该策略利用无标记生物传感器,可在近生理条件下实时监控蛋白冠的动态演化。其核心突破在于,通过精细调控微环境洗脱液的强度,首次实现了对“软冠”和“硬冠”的无损、原位逐层剥离与分别鉴定,成功捕获了这一瞬态生物界面的完整动态图谱(Nat. Commun., 2022, 13(1): 5389)。
此次刊发于Nature Protocols的研究,是在此基础上将这一技术全面升维为一套系统化的方法学框架(图1)。通过深度融合生物膜层干涉、表面等离子体共振与高分辨定量蛋白质组学,并针对纳米材料理化性质的多样性,构建了三大界面锚定策略:物理吸附保留材料原始理化特性,共价偶联抵抗复杂流体剪切,生物亲和策略实现特异性定向固定。在此基础上,实验方案按逻辑递进关系梳理为六大系统化程序:传感器功能化、蛋白冠实时动态监测、软/硬冠分层分离、高分辨质谱鉴定、动力学参数拟合及候选受体验证,实现了从微观的纳米表界面蛋白冠构成到宏观的生物学功能的闭环解析。
尤为值得关注的是,该实验平台提出了“双向映射”的前沿研究范式。它不仅能够以纳米材料表面的蛋白冠为“诱饵”,在细胞膜上原位“垂钓”未知的识别受体;也能反向利用固定化的已知受体,从复杂血浆中溯源其识别的关键蛋白组分。团队前期运用该策略,成功从脂质纳米颗粒体系中鉴定出髓系细胞表面CSF2RB受体介导的特异性吞噬机制,精准揭示了纳米药物被免疫系统快速清除的分子路径(J. Am. Chem. Soc., 2025, 147(9): 7604-7616)。
这套系统化研究策略,其意义不止于回答蛋白冠是什么,更致力于解码蛋白冠如何与细胞对话。它既是基础研究的利器,更有望成为新一代纳米药物理性设计的全新范式:让研究者得以像拨动开关一样,通过精细调控蛋白冠组分来预测和编程纳米药物的体内命运。随着纳米医学加速迈向精准临床转化,这一平台性技术将为优化免疫相容性、突破靶向递送瓶颈、精准预测体内清除速率提供不可或缺的方法学和系统化研究工具。
华南理工大学生物科学与工程学院Baimanov Didar副教授、北京大学药学院王静研究员为该文章的共同第一作者,国家纳米科学中心/中国科学院苏州纳米技术与纳米仿生研究所陈春英院士、中国科学院高能物理研究所王黎明研究员为共同通讯作者。上述研究工作得到了国家重点研发计划、国家自然科学基金、北京市自然科学基金、新基石科学基金、中国科学院建制化科研平台等项目资助。
原文链接:https://doi.org/10.1038/s41596-026-01358-6
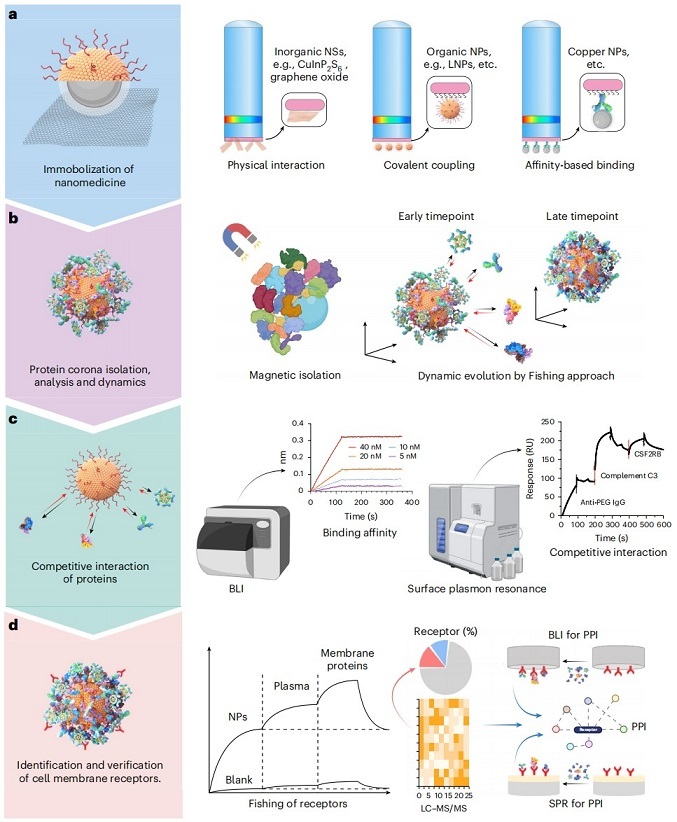
图1. 纳米材料蛋白冠分析和细胞膜受体识别的方法概述